医疗器械的设计开发过程是一个重要而繁琐的环节,其中设计确认是整个过程中不可或缺的一环。设计确认的目标是确保产品能够满足规定的应用要求或预期用途要求,通过提供客观证据,验证预期用途是否得到满足。在这一阶段,设计开发团队需要编写设计确认方案和报告,同时要注意一系列关键步骤和注意事项。
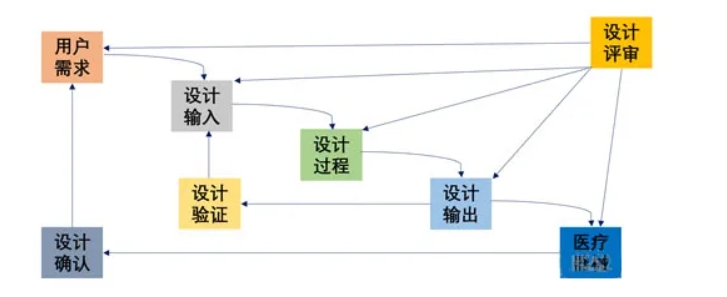
设计确认在GB/T 42061-2022中被明确定义,其核心在于通过策划并形成文件的安排,对设计和开发进行确认,以确保产品的预期用途得到满足。这涵盖了各个方面,例如产品的功能、标签和说明书的可用性、产品的有效期、临床评价、运输贮存稳定性等。
- 编写设计确认方案: 在这一步,可以根据公司内部的《设计和开发控制程序》来编写项目的设计确认方案。方案中应包括设计项目指标、被确认的样品、确认方法、接受标准、样本量原理的统计技术等。
- 编写设计确认报告: 设计确认报告是审查老师必查的文件,其中包括对每一个预期用途的确认、标签和说明书的可用性、产品有效期的确认、临床评价的确认、运输贮存稳定性的确认、生物相容性测试、软件的确认、产品接口的确认、风险分析确认等内容。
- 设计确认评审: 进行组织会审,涉及技术人员、质量人员、生产人员、法规人员、销售人员等,以确保设计确认报告的全面性和准确性。
- 选择有代表性产品进行: 选择进行确认的样品必须是采用成熟稳定工艺生产的产品批次,具有所有型号的覆盖性,并记录选择的理由。
- 与设计验证的区别: 设计验证和设计确认是两个独立但相辅相成的阶段,验证注重技术指标,而确认注重预期用途。一般是在验证后进行确认。
- 确认的产品不能放行销售: 用于确认的产品(如临床评价或性能评价的医疗器械)不能被放行给顾客使用,以防潜在的安全隐患。
- 保留记录: 应保留确认结果和结论以及必要措施的记录,以备将来的审查和追溯。
在整个设计确认的过程中,以上注意事项和步骤的合理执行将有助于确保产品的设计是合法、合规且符合预期用途的。设计开发团队应当在这一阶段严谨对待,确保产品质量和安全性,为医疗器械的后续审评和上市提供有力支持。



