
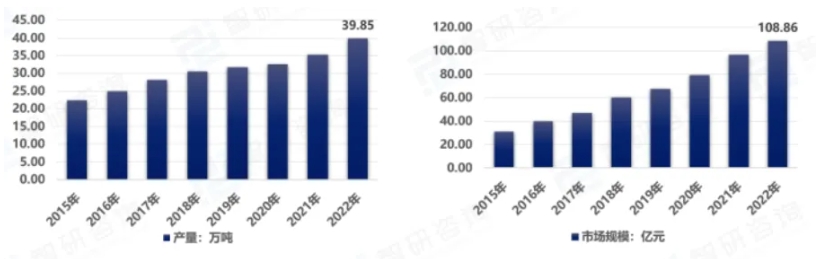
随着公众消费升级,轻医美行业的飞速发展,其产业链下游医用敷料行业也迎来了快速增长期。近年来,随着皮肤修复及护肤概念的盛行,医用敷料产品凭借适用性广、安全性高及功效性强等优势备受消费者青睐,根据智研咨询数据显示,近几年国内医用敷料产量整体呈增长趋势,产量从2015年的22.33万吨增长到2022年的39.85万吨,年复合增长率达8.63%,2022年我国医用敷料市场规模达到了108.86亿元,同比增长21.97%。
专业皮肤护理类医用敷料用户主要包括具有痤疮、皮炎等皮肤问题的患者,轻医美手术后急需皮肤修复的人群。主要的医用敷料产品如下表所示:
名称 | 预期用途 |
透明质酸敷料 | 提供创面愈合环境,用于非慢性创面的护理 |
胶原贴敷料 | 用于激光、光子术后创面修复辅助治疗 |
医用重组胶原蛋白敷料 | 用于非慢性创面(如浅表性创面、小创口、擦伤、手术后缝合创面、I度或浅II度的烧烫伤创面、激光/光子/果酸换肤/微整形术后创面)与周围皮肤的护理,为创面愈合提供微环境。 |
聚谷氨酸修护敷料 | 用于非慢性创面(如浅表性创面、手术后缝合创面、机械创伤、小创口、擦伤、切割伤创面、I度或浅II度的烧烫伤创面、激光/光子/果酸换肤/微整形术后创面)的护理,为创面愈合提供微环境。 |
医用海藻糖创面敷料 | 适用于非慢性创面(激光/光子/果酸换肤/微针治疗及微整形术后创面)的护理,为创面愈合提供微环境。 |
硅酮敷料 | 用于辅助改善皮肤病理性疤痕,辅助预防皮肤病理性疤痕的形成,不用于未愈合的伤口。 |
卡波姆湿性修护功能性敷料 | 用于非慢性创面(如浅表性创面、手术后缝合创面、机械创伤、小创口、擦伤、切割伤创面、穿刺器械的穿刺部位、I度或浅II度的烧烫伤创面、激光/光子/果酸换肤/微整形术后创面)的护理,为创面愈合提供微环境。 |
医用修护功能性敷料 (注:壳聚糖类) | 在皮肤表面形成保护层,起物理屏障作用,为皮肤屏障受损、非慢性创面提供护理。 |
临床试验研究人群的选择,取决于产品预期使用的创面类型和程度。在试验开始之前,首先应根据医用敷料的特性和作用机理、适用的创面类型等确定临床应用时的适应症人群,并根据临床试验的特点和可能的影响因素,制定入选标准和排除标准。这些标准除能够代表研究人群的特征外,还应考虑可能对临床效果评价产生影响的相关因素,并进行控制。另外,需确定产品临床应用时的禁忌人群,如对医用敷料所含成分过敏的患者及其他不适合使用的人群。
临床试验方案中应给出统计学上计算样本量大小的依据和方法。研究中所需样本量与研究目的、主要评价指标、个体间变异程度有关,还与假设检验的具体内容以及I、II类错误、组间客观差异的大小有关,不同类型研究设计对样本量也有影响。对样本量进行确定时还应该考虑到受试者退出试验以及其它可预见的偏离试验方案的情况。
敷料宣称的预期用途通常有两大类:改善伤口愈合;改善伤口护理。应根据产品宣称的预期用途选择合理的评价指标。评价指标应至少包括有效性指标和安全性指标,对不良事件和禁忌症应有处理和预防措施,以减少患者的风险。临床试验过程中还需记录创面治疗护理情况、全身或局部用药的情况、患者基础疾病控制情况等影响因素。
其中常用的评价指标,主要指标包括:创面闭合率、愈合时间、临床有效率;次要指标包括:疼痛程度、渗液量(或分泌物渗出量)、体液流失量、出血情况、产品使用是否方便、产品是否粘连伤口的新生肉芽组织、伤口愈合后质量(如愈合后疤痕情况、愈合皮肤的轮廓和感觉、皮肤斑纹或色泽的正常化)等。安全性指标:全身/局部反应及安全性、伤口感染发生率、不良事件发生率及程度。