

医疗器械外部软件环境评估报告主要包括以下内容:
安全性级别:根据医疗器械软件的安全性级别,明确外部软件环境的安全性级别。
软件标识:分类描述外部软件环境所含全部现成软件的名称、完整版本、补丁版本、发布日期和供应商信息。
功能用途:按照系统软件、应用软件、中间件、支持软件四种类型,分类描述外部软件环境所含全部现成软件的功能、用途、与医疗器械软件的关系、使用限制和选择依据。
运行环境:分类描述外部软件环境所含全部现成软件的运行环境,包括确定依据,并结合兼容性考虑医疗器械软件运行环境的确定依据。
风险管理:提供外部软件环境所含全部现成软件的风险分析报告,并附上软件开发所形成的原始文件。
验收管理:根据安全性级别的不同,概述外部软件环境的验收管理过程,提供兼容性测试计划和报告,或包括在严重级别中提供外部软件环境的兼容性测试计划和报告,以及软件开发的原始文件。
维护计划:根据安全性级别的不同,概述外部软件环境的更新管理过程,包括补丁更新、版本更新、产品更新。在严重级别中,提供现成软件停运后续维护方案,即现成软件供应商停止售后服务后的维护方案。
结论:简述外部软件环境所含全部现成软件的质量是否满足要求。
这些内容的详细程度取决于软件的安全性级别,以确保医疗器械软件的整体安全性和可靠性。
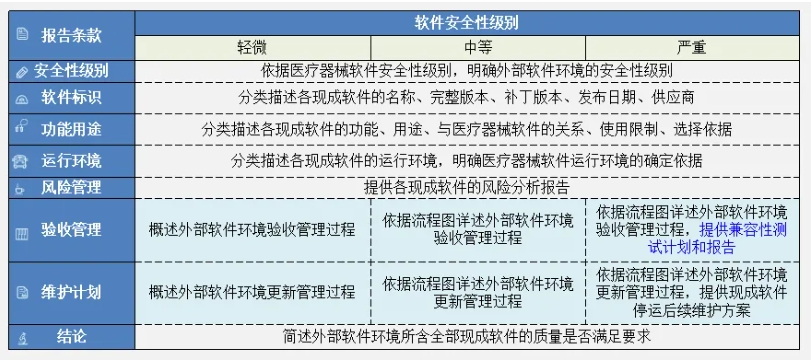
外部软件环境评估报告用于医疗器械软件外部软件环境(含云计算)的评估,适用于医疗器械软件的初次发布和再次发布,内容框架详见下表,包括安全性级别、软件标识、功能用途、运行环境、风险管理、验收管理、维护计划、结论,详尽程度取决于软件安全性级别。
(1)安全性级别
(2)软件标识
(3)功能用途
(4)运行环境
(5)风险管理
(6)验收管理
(7)维护计划
(8)结论
