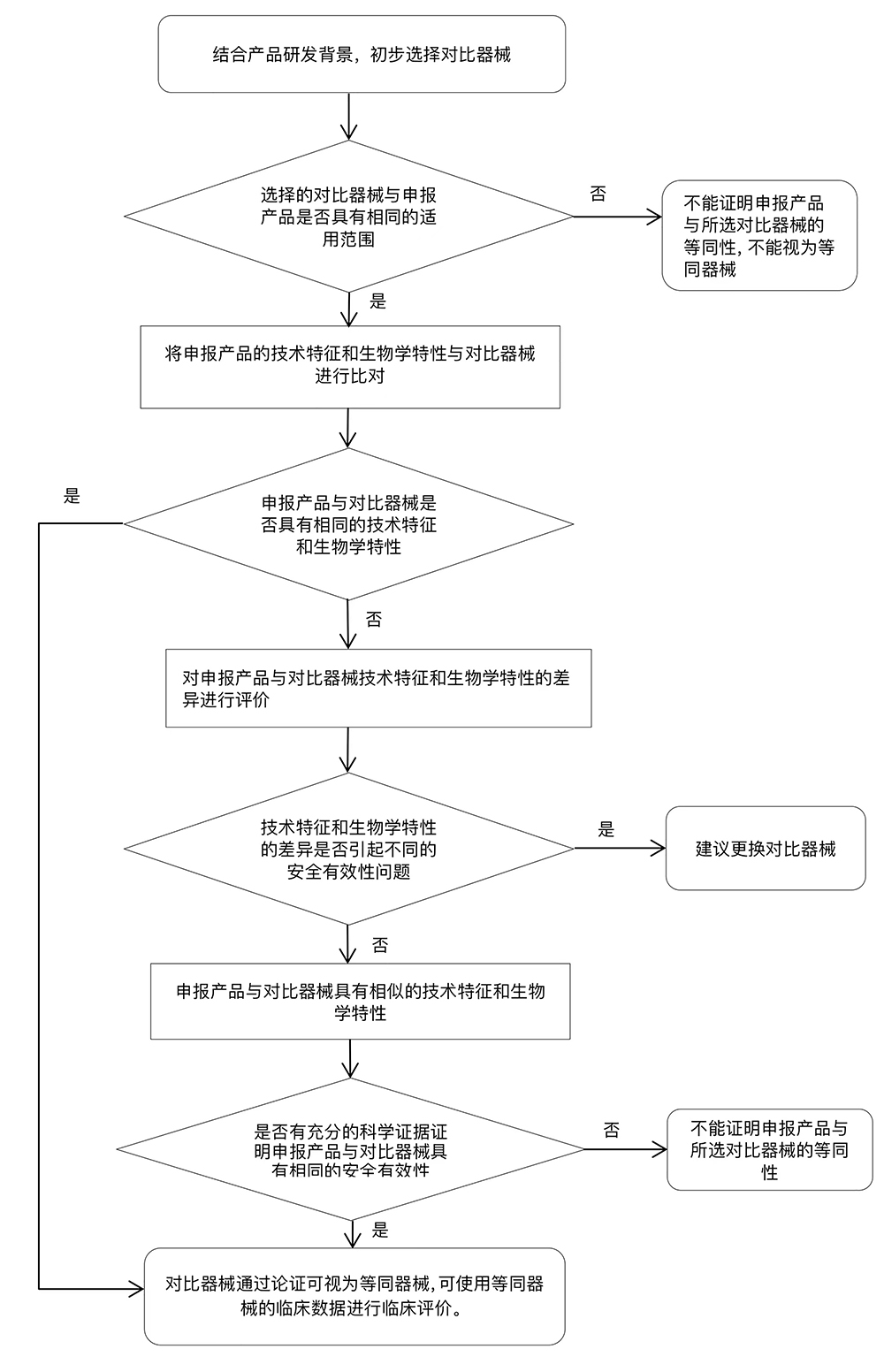
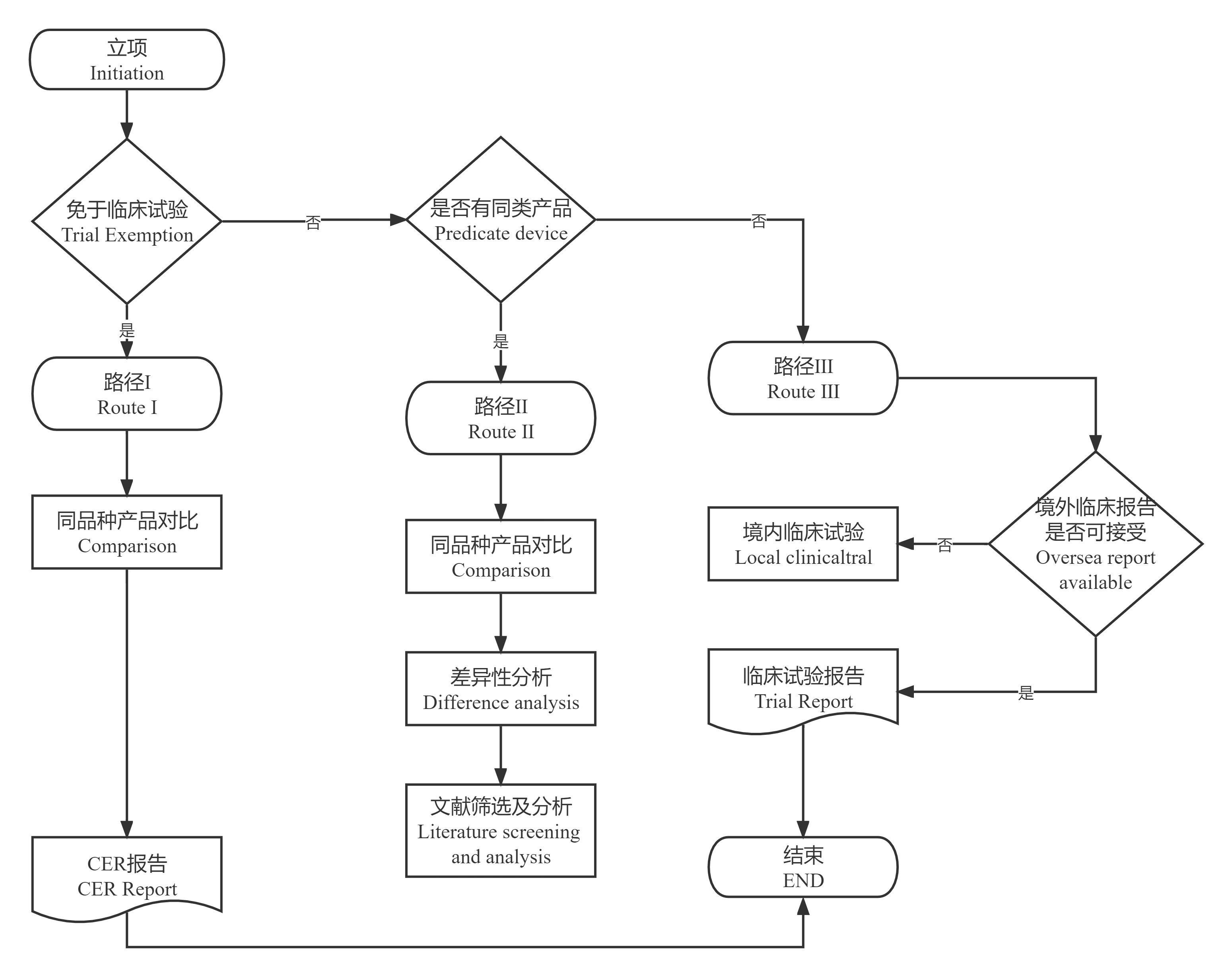
临床评价路径推荐
关于发布《医疗器械分类目录》子目录01、04、07、08、09、10、19、21相关产品临床评价推荐路径的通告(2022年第30号)
关于发布《医疗器械分类目录》子目录02、03、05、06、16、18、20相关产品临床评价推荐路径的通告(2022年第24号)
关于发布《医疗器械分类目录》子目录11、12、13、14、15、17、22相关产品临床评价推荐路径的通告(2022年第20号)
同品种临床评价指导原则
关于公开征求《髋关节假体同品种临床评价注册审查指导原则(征求意见稿)》等7项医疗器械注册审查指导原则意见的通知
关于公开征求《电子内窥镜同品种临床评价注册审查指导原则(征求意见稿)》意见的通知
有源产品:超声刀系统、钬(Ho:YAG)激光治疗机、半导体激光治疗机、二氧化碳激光治疗机、手术导航系统、射频治疗仪
温馨提示:
同品种比对临床评价法规要点:具体要根据产品结构组成、预期用途分析确定产品是否可以进行同品种比对临床评价路径。
例:超声刀系统(同品种5mm及以下)、手术导航系统(同品种如口腔种植、脊柱外科椎弓根钉置入)、射频治疗仪(用途:用于组织和器官(心脏、肝脏、前列腺、妇科和耳鼻喉等)的消融和凝固。)
不适用于按医疗器械管理的体外诊断试剂