医疗器械事关人民生命健康。UDI作为医疗器械的身份证,第三类医疗器械已经要求全部覆盖,唯一标识将逐渐覆盖所有器械。为了更好的帮助大家了解UDI,小编针对大家都比较关心的重点问题进行了整理与解答,从基础知识、相关法规标准、实施过程及步骤、数据库使用、发码机构、后续应用等方面帮助大家更好的了解UDI体系脉络。今天和大家一起分享UDI科普问答,希望对小伙伴们有所帮助!
常规应用标识符(AI)相应内容,对应关系见下表。
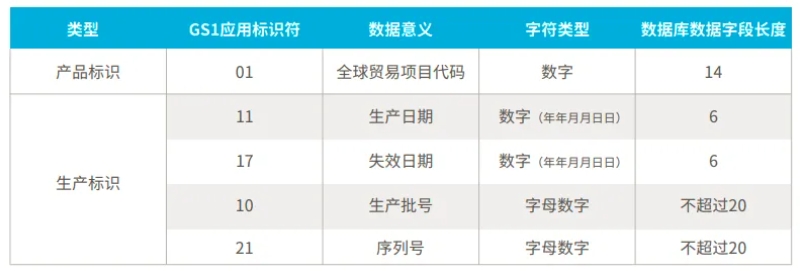
X为字母数字字符,N为数字。(编码规则详见GB/T 16986-2018 商品条码_应用标识符)(基于商品条码(GS1)标准的医疗器械唯一标识(UDI)实施指南-中国物品编码中心) http://www.gs1cn.org/Business/healthcare/UDI.aspx
具体使用组合应由风险等级及追溯数量级综合决定,其中组合过于复杂使条码过长,会引起机器扫码不流畅。
当 UDI-PI 中既有预定义长度应用标识符(如失效日期、生产日期),也有非预定义长度应用标识符(如批号、序列号)时,应将预定义长度应用标识符放在前面。规则详见《GS1 通用规范》7.8.5.3 链接使用的其他注意事项。
(1)企业可下载中国编码APP2.0,通过选择“业务办理”——“条码申请”在线办理;(2)企业可登录编码中心官方网站:http://www.gs1cn.org/,自行注册/登录用户名及密码,办理相关业务,填报业务信息;(3)企业可关注“中国物品编码中心”的官方微信,在菜单栏“业务办理”中,点击进入平台完成申请;(4)通过联系当地编码中心分支机构现场办理。
联系方式:http://www.gs1cn.org/Org/Branch.aspx 咨询电话:400-7000-690
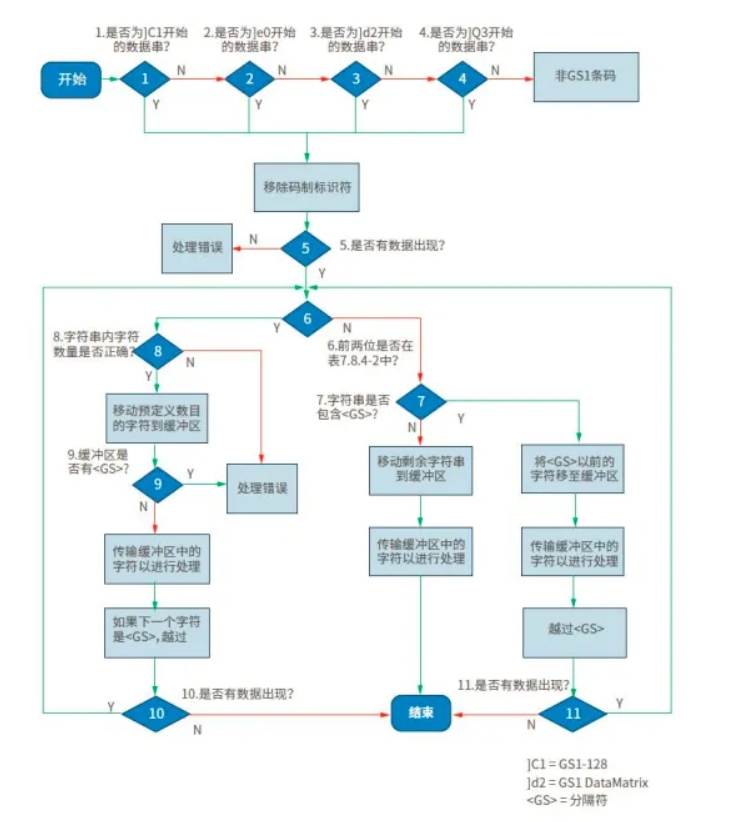
建议确认扫码设备是否设置到了识读 GS1相应条码的模式,相关软硬件是否按照GS1标准对条码进行了处理,GS1条码符号数据处理流程见下图,详见 GS1条码符号处理流程详见《GS1 通用规范》7.8。
GS1是美国、欧盟认可的UDI发码机构。在相应区域药监规定指导下,可采用编码中心分配的厂商识别代码,用于在国外销售出品产品。需要结合实际产品情况向中国编码中心咨询后结合当地法规要求后实施。
产品标识单元数据串由发码机构编码“MA”、分隔符“.”、制造商编码、分隔符“.”、产品编码组成,应作第一个单元数据串出现。产品标识单元数据串为必选项。制造商编码包含国家代码 3 位、分隔符“.” 1 位、行业代码 2 位 M0、分隔符“.”1 位、注册人代码 6 位组成。
产品编码由包装编码 1 位、项目编码 6 位和校验码 1 位组成。(医疗器械唯一标识 MA(IDcode)编码手册)
UDI-PI 可采用数据分隔符表示,对应关系见下表:
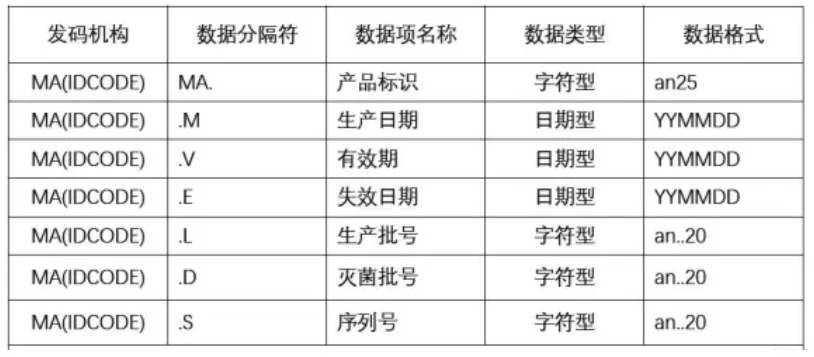
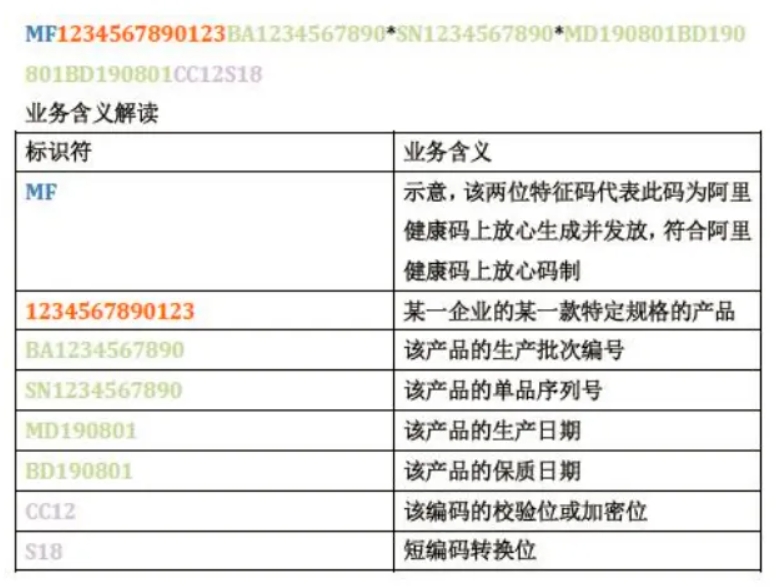
UDI 中的 DI 对应厂商标识代码+产品标识代码 UDI 中的 PI 对应产品批次信息(BN)+单品序列号(SN)+产品生产日期(MD)+产品保质日期(BD)+产品有效日期(ED)(阿里健康医疗器械唯一标识编码规范)
以下面的编码为例进行解释说明: