“创新医疗器械特别审查”与“医疗器械优先审批”是我国医疗器械监管领域两项并行不悖的政策,虽然同为医疗器械产品快速上市通道,但两者在定位与核心目标、适用范围、申请条件、办理流程、结果影响等方面有着显著差异,本期带来两者区别的详细解读,以帮助企业准确区分并应用这两种申请。
一、政策定位与核心目标对比
创新医疗器械特别审查
定位:鼓励原创技术突破
核心目标:旨在保障医疗器械的安全、有效,鼓励医疗器械的研究与创新,促进医疗器械新技术的推广和应用,推动医疗器械产业发展,强调“从0到1”的创新。
医疗器械优先审批
定位:解决临床急需问题
核心目标:旨在保障存在供应短缺或具有明显临床优势的医疗器械的临床使用需求,聚焦“填补临床空白”。
二、适用范围对比
创新医疗器械特别审查
适用范围:
仅限第二类、第三类医疗器械,且需满足以下条件之一:
1. 国际首创(全球无同类产品);
2. 国内首创(国内无同类产品获批);
3. 国产首创(仿制国外已上市产品但技术升级)。
排除情形:不适用于第一类医疗器械,或延续注册、许可事项变更。
医疗器械优先审批
适用范围:
覆盖境内第三类和进口第二类、第三类医疗器械,针对以下情形:
1. 罕见病、恶性肿瘤、儿童/老年人特有疾病且无有效治疗手段;
2. 临床急需且国内无同品种注册;
3. 列入国家科技重大专项或重点研发计划。
排除情形:已通过创新审查或应急审批的项目不再适用。
三、申请条件差异
创新医疗器械特别审查
关键条件:
1. 拥有核心技术发明专利(专利授权公告日距申请≤5年,或专利申请已公开且具备新颖性/创造性);
2. 产品已基本定型,研究数据完整可溯源;
3. 技术性能/安全性较同类产品有根本改进,且具有显著临床价值。
附加要求:需提交产品技术文件、创新证明文件(如学术论文、专利检索报告)及风险分析资料。
医疗器械优先审批
关键条件:
1. 符合罕见病、恶性肿瘤等临床领域要求,或列入国家科技计划;
2. 提供临床优势证明(如疗效显著提升、填补国内空白)。
附加要求:需同步提交注册申请与优先审批申请,并提供相关证明文件(如科技项目合同)。
四、办理流程对比
创新医疗器械特别审查
申请提交:医疗器械首次注册申请前提交,需填写《创新医疗器械特别审查申请表》。
初审与审查:
境内申请人:省级药监部门初审(20个工作日)→国家药监局形式审查→专家技术审评(60个工作日,不含公示时间)。
境外申请人:国家药监局形式审查→专家技术审评(60个工作日,不含公示时间)。
公示与异议:公示期≥10个工作日,接受异议。
医疗器械优先审批
申请提交:与医疗器械注册申请同步提交,需填写《医疗器械优先审批申请表》。
初审与审查:国家药监局形式审查→专家论证。器审中心每月集中组织专家论证审核,出具审核意见。(对列入国家科技重大专项或国家重点研发计划的医疗器械,器审中心自收到申请之日起5个工作日内进行审核)
公示与异议:公示期≥5个工作日,接受异议。
注:以上仅指国产三类、进口三类和进口二类医疗器械的创新及优先审批流程,国产二类器械的相关流程在其所在地的省级药品监督管理部门进行受理,相关流程时限上各地略有差异。
五、结果影响
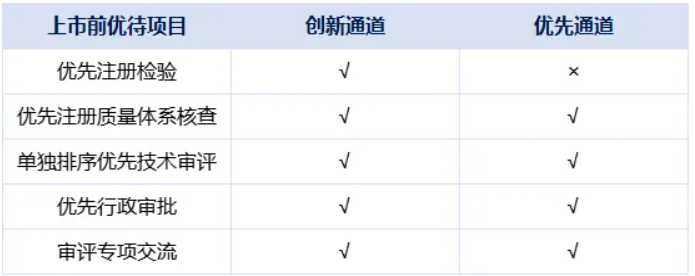
六、核心差异总结
定位不同:创新审查聚焦“技术领先性”;优先审批聚焦“临床急需性”。 适用范围不同:创新审查仅限国内首创的第二类/第三类器械;优先审批覆盖更多临床领域及进口器械。 申请条件不同:创新审查强调专利与技术创新;优先审批强调临床优势与国家项目支持。 审批流程不同:创新审查需专家技术审评;优先审批通过专家论证后优先处理。 结果影响不同:创新审查可获得更早的技术指导,降低研发风险;优先审批主要是缩短注册审评时间。
七、企业选择建议
两项政策共同构成我国医疗器械创新的“双轨道”支持体系:
创新审查为原创技术提供“绿色通道”,助力高端医疗器械国产化;更适合技术突破性强、研发风险高的项目,需早期与药监部门沟通优化方案。
案例--首个国产人工心脏(2019年通过创新通道获批)。
优先审批为临床急需产品开辟“快速通道”,保障患者可及性。更适合临床需求明确、数据成熟的产品,需快速上市以抢占市场。
案例--新冠检测试剂(2020年通过优先通道紧急获批)。
企业可根据产品特性选择适合的路径,或同时符合多项政策时,优先审批不排斥创新审查(但已通过创新审查的项目不再适用优先审批)。
八、全国医疗器械创新与优先审批现状
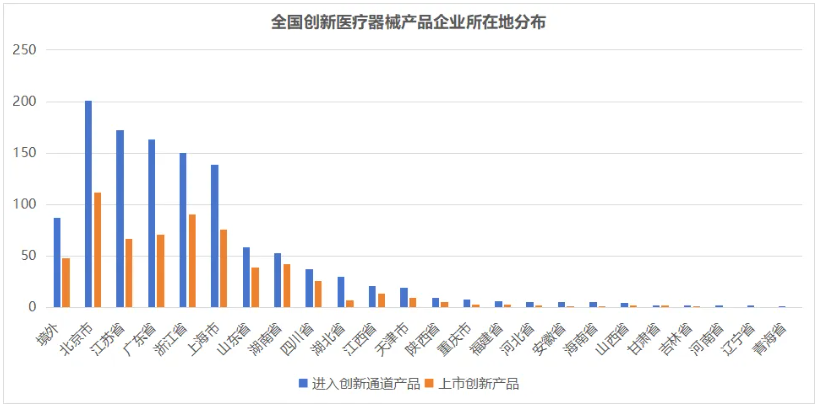
据药智医械数据统计,2014年至2025年4月,全国共有1181个产品进入创新特别审批通道(包括国产产品1094个,进口产品87个),其中已获批上市的620个(国产产品572个,进口产品48个)
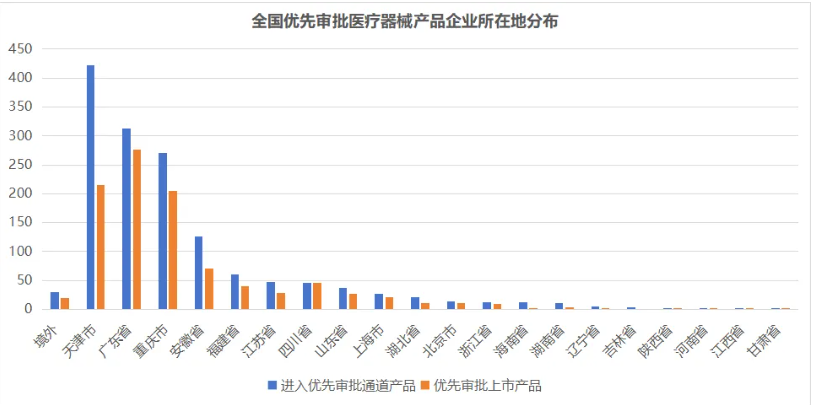
同时全国共有1460个产品进入优先审批通道(包括国产产品1431个,进口产品29个),其中已获批上市的990个(国产产品971个,进口产品19个)