

01、美国医疗器械定义
美国的医疗器械监管部门是U.S. Food&Drug Administration,美国食品药品监督管理局,简称FDA。
官方网站:https://www.fda.gov/
美国的医疗器械(Medical Device)定义:
根据《食品、药品和化妆品法》第201(h)节,医疗器械为:仪器、设备、器具、机器、用具、植入物、体外试剂或校准器,或者其他相似或相关物品,包含零部件或配件,它是∶
记载于正式的国家处方集,或美国药典,或其附录;
疾病的诊断、监护、缓解、治疗或预防,作用于人类或其他动物;(“器械市场”备注:这点与中国不同;中国的医疗器械不包括动物用的)
影响人体或其它动物身体的结构或功能,并且不是通过在人体或动物体内的化学作用,也不是依靠产生代谢变化来获得既定预期用途。
英文原文:
Per Section 201(h) of the Food, Drug, and Cosmetic Act, a device is:
An instrument, apparatus, implement, machine, contrivance, implant, in vitro reagent, or other similar or related article, including a component part, or accessory which is:
recognized in the official National Formulary, or the United States Pharmacopoeia, or any supplement to them,
intended for use in the diagnosis of disease or other conditions, or in the cure, mitigation, treatment, or prevention of disease, in man or other animals, or
intended to affect the structure or any function of the body of man or other animals, and which does not achieve its primary intended purposes through chemical action within or on the body of man or other animals and which is not dependent upon being metabolized for the achievement of its primary intended purposes.
02、FDA对医疗器械的分类
FDA将医疗用品分为三类,并采取不同的管理和控制:
(1)第一类医疗器械Class I:低等风险(监管控制类型:基本控制)
产品必须合乎一般规定要求,大部分可以直接注册,无需递交产品安全有效性报告;
(2)第二类医疗器械Class II:中等风险(监管控制类型:基本控制以及特殊控制)
产品必须达到功能标准;大部分需要注册前向FDA递交FDA510(K) (PMN市场预投放通告)的产品本身的安全有效性论证报告,获批后才可以进行产品注册和合法上市销售;申请周期在半年以上;510(K)仅对产品进行书面论证,不涉及获批前的工厂质量体系FDA GMP QSR820的现场审核;
(3)第三类医疗器械Class III:高等风险(监管控制类型:基本控制以及上市前批准)
最严格控制,上市前必须先经批准。大部分需要先申请FDA PMA市场预投放批准,获批后才可以进行产品注册和合法上市销售;申请周期在一年以上;获批前FDA会对制造商进行FDA GMP QSR820质量体系的现场审核,通过后才可获批该产品的PMA申请。
03、美国医疗器械的相关法规
美国法典CFR(CODE OF FEDAL REGULATION)的第21篇食品和药品中对医疗器械的通则、标签、分类、注册、豁免、召回等环节的标准、要求作出了详尽的规定。
官网链接:https://www.ecfr.gov/current/title-21/chapter-I/subchapter-H
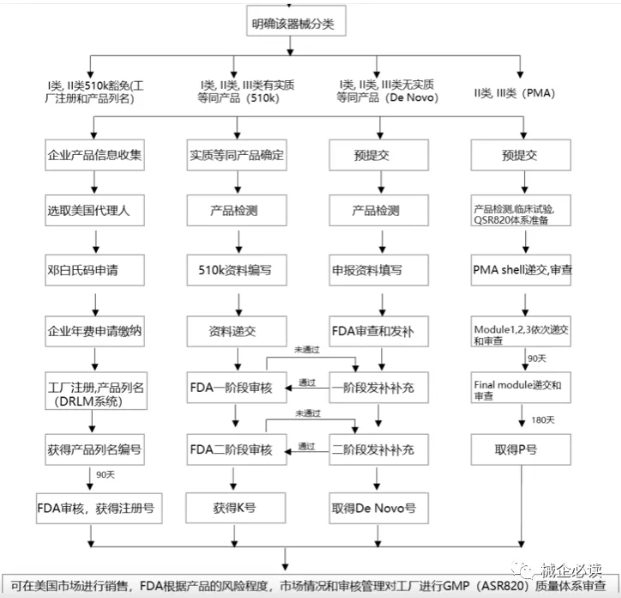
04、FDA医疗器械注册程序
(一)选择正确的路径递交
器械分类确定之后,需要选择相应法规要求下的上市前递交。常见的上市前递交类型包括:
• 510(k)(上市前通知)
• PMA(上市前批准)
• De Novo(自动III类指定的评价)
• HDE (人道主义器械豁免)
Ⅰ类以及大部分Ⅱ类器械要求以510(k)的方式递交。在510(k)递交过程中,申请者必须证明新的器械与对比器械在预期用途,技术特征以及性能测试方面实质等同。一些Ⅰ类和Ⅱ类器械可以豁免510(k),如果他们在21 CFR 862-892.9所述的豁免范围之内。这些豁免被列在21 CFR的分类规则中,也被汇集在医疗器械豁免文件中。
大部分Ⅲ类器械要求的递交方式为PMA。PMA为严格程度较高的上市前递交类型。在FDA批准PMA之前,申请者必须提供有效的科学证据,以证明器械预期用途的安全性以及有效性。
De Novo为没有有效对比的新器械提供一种方式,如果这种新器械满足特定标准,可以被分为Ⅰ或Ⅱ。
HDE为Ⅲ类器械提供了一种监管路径,这类器械预期对罕见疾病或状况的患者是有益的。器械有资格成为人道主义豁免器械,申请者必须获得人道主义使用器械(HUD)的指定,可通过向FDA的孤儿产品开发办公室Office of Orphan Products Development (OOPD)递交申请。
(二)准备材料
在选择正确的上市前递交类型之后,必须准备该递交类型所需的适当的资料。FDA开发一些帮助申请者准备上市前递交的资源类型,包括:
1.器械建议(Device Advice):—综合基于FDA上的网页法规协助
2.510(k)的准备:参考Premarket Notification 510(K)
3.PMA的准备:参考Premarket Approval (PMA)
4.CDRH学习(CDRH Learn):基于视频的教学模块,研讨会和录制的包括各种政策和指导力度的网络研讨会,CDRH递交前程序 —未来上市前提交申请可能要求FDA通过这个程序进行反馈。
准备上市前递交时需要考虑的信息:
(1)设计控制:所有II类以及III类器械根据质量管理体系(21 CFR 820.30)中对设计控制的要求进行设计。一些I类器械可豁免设计控制。
(2)非临床测试:器械上市要求的测试以及信息类型是通过器械的分类,作用机制,技术特征,以及标签来确定的。医疗器械上市前递交实施的非临床测试必须符合21 CFR 58中的良好试验管理规范(GLPs)
(3)临床证据:PMAs,HDEs 以及部分 510(k)s 和 De Novos 要求有临床证据。在早起的临床研究开始之前,研究申请者需要得到FDA器械临床研究豁免(IDE)的批准。这项研究也需要得到伦理审查委员会(IRB)的批准。临床研究必须符合所有的适用的器械临床研究豁免(IDE)法规以及良好试验管理规范(GLPs)。
(4)标签:器械的标签必须依据标签法规书写,且需要包含在上市前递交的资料中。
(三)递交资料
提交给FDA,并在FDA的工作人员审查过程中保持联系。
1.用户费用:在510(k)或PMA递交时,需要一定的用户费用
2.电子副本(eCopy):上市前递交必须包含以光盘(CD)、数字视频光盘(DVD),或闪存驱动器方式形成的电子副本。
3.行政备案审查:在上市前递交接收之后,FDA进行行政审查,评估递交是否是足够完整的,以接收实质性审查。
4.审查互动(Interactive Review):当递交的资料处于正在审查中时,FDA将和申请者保持联系以增加审查过程中的效率。
(四)完成登记
器械设备必须在FDA对其生产的企业进行登记,并对其器械进行列名。如果一个器械在上市前需要上市前清关(premarket clearance)或上市前批准(premarket approval),器械厂商在登记和列名之前必须等到它获得FDA的清关或批准。器械企业登记、登记号的分配或医疗器械的列名,都不意味着FDA对其企业或其产品的清关或批准。
