以聚乳酸(PLA)、聚己内酯(PCL)及聚丙交酯-乙交酯(PLGA)为代表的生物可降解聚酯材料,其核心优势在于其卓越且可设计的性能。这些材料不仅具备与人体良好的生物相容性,能避免持续炎症反应并最终降解为无毒产物被机体代谢,还拥有可精准调控的降解周期与匹配组织需求的机械性能。此外,它们也展现出优良的加工适应性。上述所有特性均受到材料自身的化学与物理特性深刻影响,包括分子量、亲疏水性、表面电荷及降解机理等,因此可以通过分子设计来精准定制,以满足特定生物医学应用的需求
01、生物相容性
可降解聚酯材料的安全性根植于其卓越的生物相容性。这体现在材料本身及其降解产物均能与生物体和谐共存:材料在与活体组织、血液或体液接触时,能有效执行其设计功能,而不会引发有害的局部或全身反应;其降解产物则可被机体安全地吸收或排出。例如,聚乳酸(PLA)的降解终产物是乳酸,该分子是人体内天然的代谢中间体,能够顺利进入三羧酸循环(TCA cycle)被彻底代谢,最终生成二氧化碳和水,并经由呼吸、泌尿等生理途径排出体外,从而实现其在体内的完全清除。
02、可调控的降解性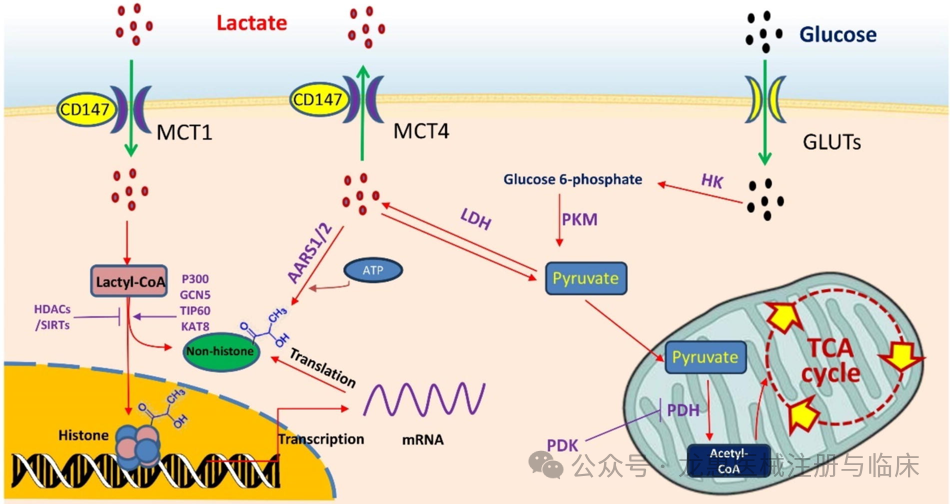
生物可降解聚酯材料的关键优势在于其降解行为可被精确调控,以匹配组织再生的内在节律。它在体内充当“临时支架”时,其降解(包括表面侵蚀与本体侵蚀两种模式)不仅是物理上的消失,更是在主动调控修复微环境与再生进程。通过调控单体组成、分子量、结晶度等参数[2],可将材料在体内的存留时间精准设计在数周至数年之间,从而满足从短期皮肤填充(3-6个月)到长期深层支撑(12-24个月)等不同组织的再生需求。
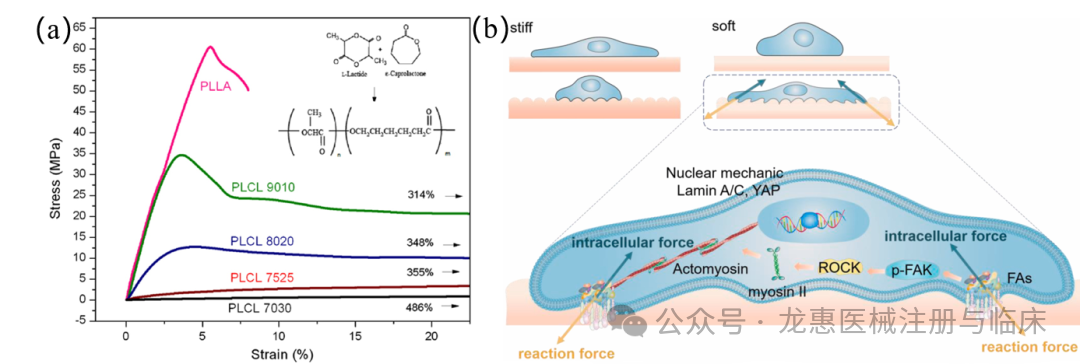
03、可调控的机械性能 生物可降解材料的临床成功,关键在于其力学性能能否与目标组织实现动态适配。与传统惰性植入物不同,它们必须在组织修复期内提供适时、适地的力学支撑,并随新生组织的长成而逐步功成身退。这要求材料的模量、强度及降解行为具备“时-空-力”三位一体的可设计性。 借助分子工程手段(如调控PLA/PCL/PGA共聚比例、链结构、结晶度)及非均相织态构建技术,可实现从模拟软组织的柔性凝胶(其柔软基质通过改变局部力学环境与结合位点密度,优化细胞粘附与力信号转导)到仿骨结构的刚性支架的宽域力学性能定制。例如,脂肪替代材料需具备低模量(<1MPa)与高延展性,而下颌角塑形材料则需数百MPa的模量以维持结构稳定。 因此,再生医美材料的设计核心已演进为“功能导向的力学适配”:即依据特定部位的解剖功能、修复周期与力学微环境,逆向设计材料结构,实现力学支持的“按需分配”与“动态演化”,从而在确保安全的同时,达成最优的美学与功能重建。 04、优异的加工性能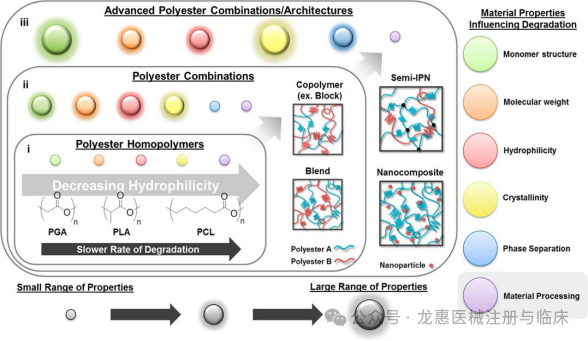
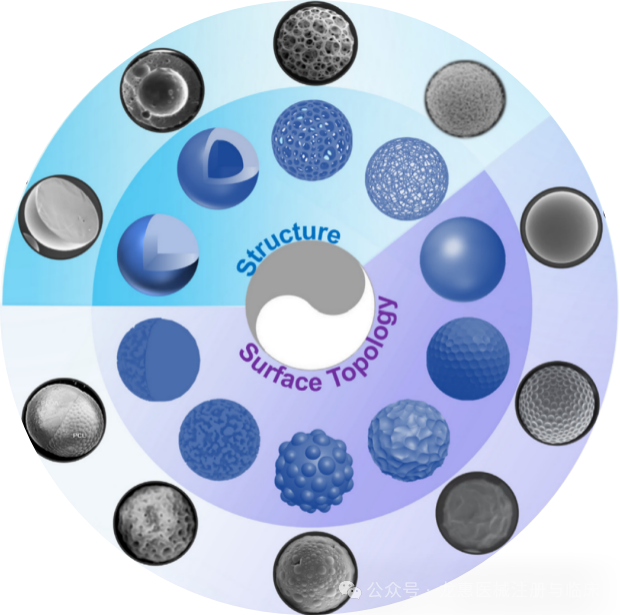
在再生医学、药物递送与高端医美领域,可降解聚酯材料正展现出广阔的设计与创新前景。这得益于其卓越的加工适应性,能够灵活兼容多种先进制造工艺,从而精准构建出尺度横跨纳米至厘米级别的复杂结构(从微纤维到定制化植入体)。如下图所示,即为通过不同工艺制备出的、具有各异结构与形貌的可降解聚酯材料微球。