

在医疗器械研发与注册过程中,产品检验报告是不可或缺的关键文件。随着我国医疗器械监管体系的不断完善和创新驱动发展战略的深入实施,医疗器械产品检验报告的形式和要求也发生了显著变化。2021年新版《医疗器械注册与备案管理办法》的发布,标志着我国医疗器械监管进入了一个更加灵活、高效的新阶段。下文将系统解析医疗器械产品检验报告的三种主要类型——注册检验、委托检验和注册自检,帮助医疗器械企业根据自身情况选择最适合的检验路径,提高产品注册效率,降低合规风险。
一、医疗器械产品检验报告概述 医疗器械产品检验报告是证明产品符合安全性和有效性要求的重要技术文件,是开展临床试验、申请产品注册或备案的前提条件。传统上,医疗器械注册必须提供由国家认可检测机构出具的注册检验报告。但随着行业发展和监管创新,检验报告的形式已呈现多元化趋势。 根据新版《医疗器械注册与备案管理办法》(2021年8月26日公布),医疗器械产品检验报告可以是: 医疗器械注册申请人或备案人的自检报告 委托有资质的医疗器械检验机构出具的检验报告 传统的注册检验报告 这一重大调整为医疗器械企业提供了更多选择空间,体现了"放管服"改革精神和鼓励产业创新发展的政策导向。 二、三种检验报告类型详解 1. 注册检验报告 定义与特点:注册检验是指由国家药品监督管理局认可的、具有医疗器械检验资质且检验项目在其承检范围内的医疗器械检测机构,依据产品技术要求对申报产品进行的全项目检验。注册检验报告具有最高权威性,是传统医疗器械注册的"黄金标准"。 执行机构:目前国家药监局认可的有资质的检验机构共有53家,其中国家级检验机构10家。这些机构通常隶属于药监系统,具备深厚的专业积累和公信力。 优势与局限: 优势:报告权威性强,100%获得药监部门认可;不收取检验费用 局限:需排队候检,周期长且不确定;检测机构资源有限,难以满足行业快速增长的需求 适用情况: 高风险类产品(如三类植入器械) 创新医疗器械特别审批程序中的产品 企业对其他检验方式信心不足时 2. 委托检验报告 定义与特点:委托检验是指企业委托具有资质的检验机构(不限于药监系统),依据标准和产品技术要求对产品进行检验并取得报告的过程。这是一种商业化服务模式。 执行机构范围: 药监系统认可的检测机构 具有检验检测机构资质认定证书(CMA)及相应能力的第三方机构 承检范围内有对应标准的检测机构 优势与局限: 优势:周期相对注册检验更快;可选择专业领域匹配的检测机构 局限:商业性质,需支付服务费用;部分第三方机构能力可能不足,报告认可度存在风险 选择建议: 优先选择药监系统内检测机构 如选择第三方,需严格评估其资质、能力和历史表现 提前与监管部门沟通确认报告认可可能性 适用情况: 时间要求紧迫的项目 专业性较强的特殊产品 注册检验资源紧张时的替代方案 3. 注册自检报告 定义与特点:注册自检是指医疗器械注册申请人按照产品技术要求,自行或委托受托生产企业对其申报产品进行全项目检验并出具报告。这是新版法规引入的重大创新。 政策依据:《关于医疗器械注册自检管理规定》(国家药监局公告第126号,2021年10月21日)对自检工作进行了详细规范。 实施要求: 企业需具备相应检验能力(人员、设备、设施和环境) 自检工作需纳入质量管理体系 将接受医疗器械质量管理体系核查 优势与挑战: 优势:最大程度掌握主动权;节省外送检验时间和成本 挑战:企业需投入建设检验能力;承担更多主体责任和风险 适用情况: 大型医疗器械生产企业 产品线稳定、检验能力成熟的企业 常规性、风险可控的产品 三种检验报告的比较分析 三、企业选择策略建议 风险评估优先:高风险产品建议优先考虑注册检验或药监系统内委托检验 能力匹配原则:根据企业自身检验能力建设情况理性选择 效率成本平衡:权衡时间成本、经济成本和机会成本 动态调整策略:随着企业发展和产品变化调整检验策略 提前沟通确认:重大变更前与监管部门充分沟通 结语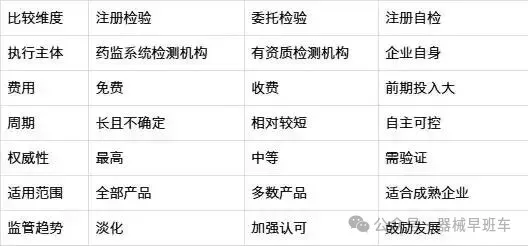
医疗器械产品检验是确保患者安全的重要关口,也是企业产品上市的关键环节。新版法规下,检验报告形式的多元化为企业提供了更多选择,同时也对企业的主体责任意识和质量管理能力提出了更高要求。医疗器械企业应当深入理解政策精神,客观评估自身条件,科学选择检验路径,构建与产品特性和发展阶段相匹配的检验策略。未来,随着监管体系的不断完善和行业成熟度的提高,我国医疗器械检验体系必将更加科学、高效,为医疗器械创新和产业高质量发展提供坚实支撑。
