长期以来,人因工程一直应用于航空航天、核能、石化、能源和运输等高危行业,以尽量减少潜在风险。生命科学行业中的人因工程越来越被认为是一个重要的话题。虽然人因工程以前只被接受为具有复杂用户界面的电子医疗设备所必需的,但它已经发展成为全球大多数医疗产品开发的强制性设计输入要求。
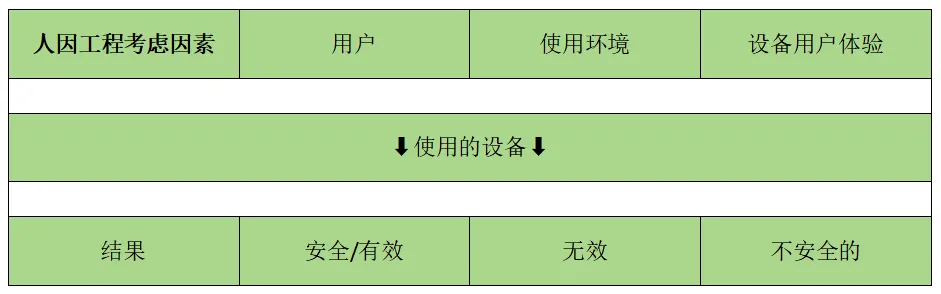
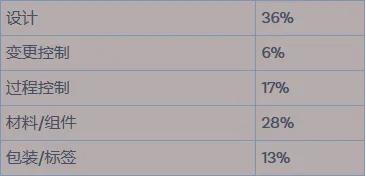
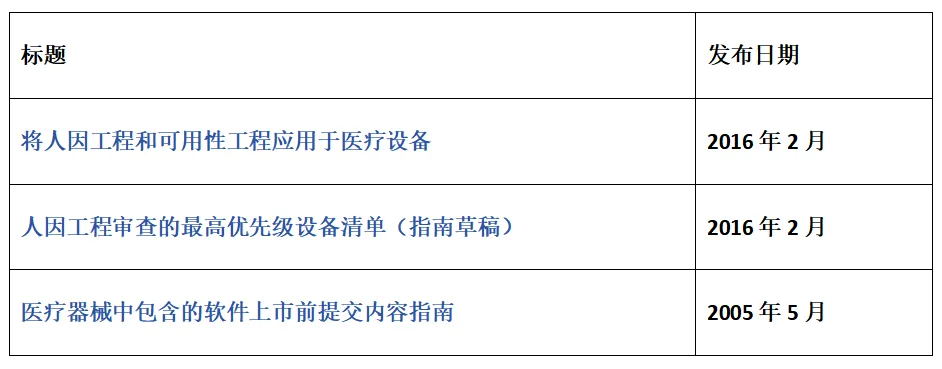
人因工程:他为什么对患者很重要 大量医疗设备被用于危重患者监测,使用中的错误导致患者受到伤害,已逐渐成为制造商和患者关注的主要因素。此类错误的因素通常是由于设备用户界面设计不佳,尤其是在涉及复杂用户系统的情况下。 输液泵、呼吸机、自动电子除颤器和药物设备组合产品(例如自动注射器)被认为可能存在与用户界面相关的问题,这些问题可能导致严重的危害,例如过量服用和危险的延迟或药物输送困难。 医疗设备的功能越来越多样化,并且在繁忙的环境中使用频率越来越高,有新的干扰和对专业培训的要求。随着患者护理的发展并转移到私人住宅或公共环境,必须使包括患者和护理人员在内的技能较低甚至不熟练的用户能够安全地使用这些复杂的设备。 图 1:人因工程影响使用医疗器械的结果(摘自 FDA 将人因工程和可用性工程应用于医疗器械,FDA 2016) 监管框架内的可用性工程 美国食品和药物管理局(FDA)每年收到约100,000份医疗器械事故报告。这些报告中有三分之一以上被认为主要归因于用户错误。这一数字与FDA公布的2003财年至2012财年医疗器械召回趋势数据分析相关[4]。 图2:美国FDA召回,按类别划分(2003财年-2012财年) 引用的报告得出的结论是,虽然与设计相关的故障一直是医疗器械召回的主要原因,但对过去三 (3) 年趋势的回顾表明,器械设计召回的百分比保持稳定。 评估召回的最常见原因 – 软件设计失败 医疗器械软件可以存在于设备本身中,也可以用于制造医疗器械。医疗产品越来越依赖软件,似乎对软件的微小更改会对设备功能和临床性能产生重要影响。如果未能在适当的情况下(增加连接性和互操作性)实施软件设计控制测试程序以增加环境用户复杂性,则可能导致软件异常,通常需要更正或删除。 由于这些趋势,FDA发布了几份新的指导文件,以强调在医疗设备和系统的设计和开发中需要人因工程,包括: 已出台的国际质量管理体系标准“ISO13485:2016 强调了可用性工程作为强制性设计输入的必要性。其他相关部分是指可用性要求的输出,例如所需的用户培训,以确保医疗设备在其预期环境中的指定性能和安全使用。 医疗器械设计和开发的人因工程设计和可用性工程要求也明确实施到当前和即将出台的欧盟监管指令框架中。 2010 年,指令 2007/47/EC [6] 修订了医疗器械指令 (MDD),第 18 条为在 MDD 中引入更具体的人因工程(即人体工程学要求)提供了背景:随着患者安全计划的设计在公共卫生政策中发挥着越来越大的作用,有必要明确规定在基本要求中考虑人体工程学设计的必要性。此外,应在基本要求中进一步强调用户的培训水平和知识水平,例如非专业用户的情况。 制造商应特别强调产品可能被滥用的后果及其对人体的不利影响。 (注意:指令中的术语“误用”在本文档中最好解释为“用户错误”,这与上述定义的“异常使用”截然不同。) MDD [7] 附录 I 中的基本要求 (ER) 包括对人因工程的具体要求,如下所述。这些基本要求也与作为药品监管的药物-器械组合产品的器械组件有关(参见MDD:M5第1.3条): 预期 1:设备的设计和制造方式必须确保,当在预期条件下和目的下使用时,它们不会损害临床状况或患者的安全,或用户或(如适用)其他人的安全和健康,前提是可能与其预期用途相关的任何风险在与患者益处权衡时构成可接受的风险,并且与高度保护健康和安全。 这应包括: 尽可能降低由于设备的人体工程学特性和设备使用环境[1]而导致的用户错误风险(为患者安全而设计);和 考虑技术知识、经验、教育和培训,并在适用的情况下考虑目标用户的医疗和身体状况(为非专业人士、专业人士、残疾人或其他用户设计)。 ER 9.2:与其物理特征相关的受伤风险,包括体积/压力比、尺寸和适当的人体工程学特征; ER 10.2:测量、监控和显示刻度的设计必须符合人体工程学原则,同时考虑到设备的预期用途; 预期成果 13.1:每个设备都必须附有安全、正确地使用它所需的信息,同时考虑到潜在用户的培训和知识,并确定制造商;和 其他可能受人因工程设计间接影响的 ER 包括 2、3、6、12.8和 12.9. 新的欧盟医疗器械法规 MDR/2017/745 [7] 进一步规定了人因工程/可用性工程的必要性。附件 1,安全和性能要求的一般要求,在第 5 节中规定: 在消除或降低与使用错误相关的风险时,制造商应: 尽可能降低与设备的人体工程学特征和设备使用环境相关的风险(为患者安全而设计),以及 考虑技术知识、经验、教育、培训和使用环境(如适用),以及目标用户(为非专业人士、专业人士、残疾人或其他用户设计)的医疗和身体状况。 MDR第1(12)条 被视为指令 2006/42/EC [1]第 2 条第 (a) 款第 (a) 点含义内的机械的设备,如果存在该指令规定的相关危险,也应满足附件 I 中规定的基本健康和安全要求。如果这些要求比本法规附件一第二章中规定的一般安全和性能要求更具体,则应这样做。 2006/42/EC(机械指令)附件 1 [8] 在预期的使用条件下,必须将操作员面临的不适、疲劳以及身心压力降低到尽可能少,同时考虑到人体工程学原理,例如: 考虑到操作员的身体尺寸、力量和耐力的变化, 为操作员身体各部位的运动提供足够的空间, 避免机器决定的工作率, 避免需要长时间集中注意力的监测,以及 使人/机械界面适应操作员的可预见特征。 产品生命周期和持续改进 为了满足当前和未来严格的监管要求,可用性工程必须在产品设计和开发中进行规划、实施和验证,从概念阶段到设备的最终验证,甚至在上市后阶段。(上市后监督 (PMS) 被定义为对所有医疗器械/IVD 以及与药物一起使用的医疗器械组合进行持续收益-风险分析的一部分。 考虑到医疗器械和药物器械组合产品的广泛性,根据器械类型、预期用途和类似器械的已知用户错误,有必要对监管要求采取灵活的方法。但是,所采取的方法应基于风险,合理并在整个产品生命周期中适当记录。 MDR概述了制造商第83条上市后监督系统持续改进的概念。第 3 节 f) 明确要求 PMS 数据应用于“确定选项,以提高设备的可用性、性能和安全性”。 最佳的行业实践是在产品的整个生命周期中不断改进用户界面。在整个产品生命周期中,需要一个强大的变更管理流程,以有效地处理用户界面的变化,无论是来自关键试验数据、上市后监督的反馈,还是由于组件供应问题而获得的信息。 最佳临床结果通常通过总结性测试/设计验证、风险管理和上市后警惕来实现。考虑因素包括人因工程,例如对自己和类似设备的上市后监控、设备/用户界面、客户洞察、人种学研究、医疗保健提供者培训以及事件分析和报告。设备制造商还可以从进行 MD/IVD 收益风险分析中受益,包括识别使用、用户环境、使用和用户错误的风险评估、与安全相关的任务和用户界面的优先级,以及进行形成性测试和设计迭代。 结论:这一切意味着什么? 对安全有效的医疗器械的监管要求在不断变化,但大多数新兴框架都要求对人因工程/可用性工程进行更强大、更深入的考虑,以确保患者在市场准入之前及以后的安全和临床表现。 在所有产品开发阶段(临床前测试、临床调查、市场准入和后期生产)中,仔细讨论和评估潜在用户群体的可用性设计输入因素以及设备的预期用途将变得越来越重要,并记录所采用方法的合理性。 在开发用于市场准入和持续商业接受的医疗设备时,不能再忽视或忽视设备可用性差的问题。